文|氨基观察
RSV(呼吸道合胞病毒)疫苗百亿市场的争夺战,一触即发。
上周,辉瑞、葛兰素史克研发的RSV疫苗,先后获得了FDA疫苗与相关生物制品产品咨询委员会支持,推荐这两款疫苗适用于60岁以及上的成年人。
屡战屡败六十年,RSV疫苗终于要迎来零的突破。不出意外,两个多月后,我们就能看到第一款RSV疫苗的诞生。
一切,都是基于辉瑞、葛兰素史克在2022年发布的三期临床数据,同样研发上岸的还有Moderna。
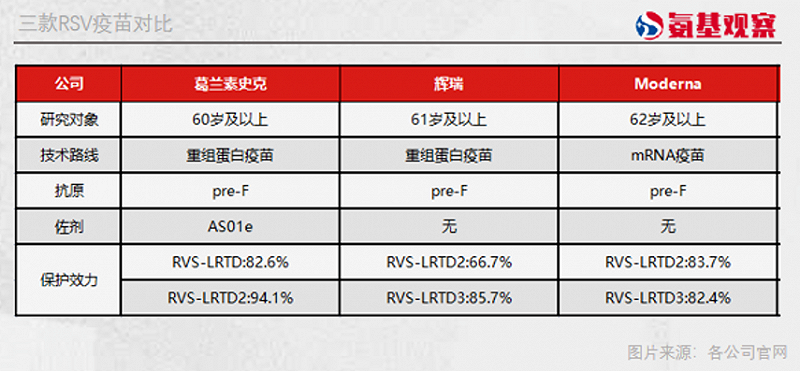
希望与挑战同在。这三款疫苗虽未进行头对头试验,但如果以预防2种或更多RSV相关下呼吸道症状(RVS-LRTD2)的有效率作为统一临床终点,辉瑞、Moderna、葛兰素史克疫苗保护率分别为66.7%、83.7%、94.1%。
从以上数据来看,在新冠上表现超凡的mRNA技术,这次没能给Moderna的RSV疫苗带来效果加成;而辉瑞、葛兰素史克的两款重组蛋白疫苗,虽是同一技术路线,保护效果却大相径庭。
在同一领域的相同路线上,大药厂却碰撞出不同的火花。那么,影响RSV疫苗效果的核心因素,到底是什么?这又会给后来者带来什么经验参考?
2023年,注定载入RSV疫苗研发史册。分野就在2023年。
01 决定生死的抗原
抗原的选择是决定一款疫苗有效性的重要原因。
如果选择了合适的抗原,人体就可以产生体液或/和细胞免疫,让病原体失去致病力,从而成功抵御病毒。相反,如果选择不合适的抗原,虽在一定概率上也会产生免疫应答,但这种免疫力很可能无法对病原体起效。
过去,在RSV疫苗的抗原选择上,研究人员就走了很多年的弯路。
在RSV的8种结构蛋白中,F蛋白是研制RSV疫苗的首选抗原,但相对稳定的F蛋白并没有想象中那么好搞定。
随着研究的深入,科学家发现,F蛋白有两幅“面孔”。在感染人体之前,F蛋白处于融合前(pre-F)的亚稳态结构,而在感染人体后,F蛋白又会不可预测地转换为另一种稳定的融合后(post-F)结构。
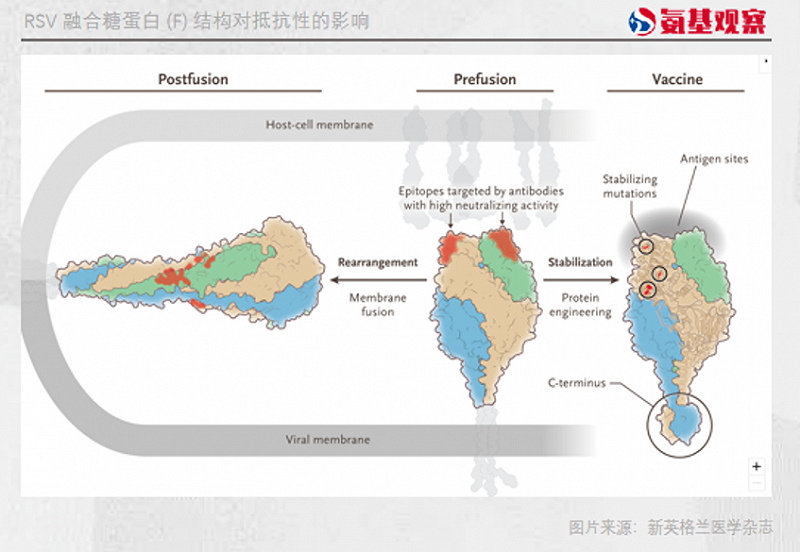
由于post-F蛋白更稳定,所以第一代RSV疫苗,基本都选择post-F蛋白作为抗原。比如RSV疫苗领域的先驱Novavax,最早研发的一款ResVax疫苗,选择的抗原便是post-F蛋白。
遗憾的是,在临床试验中,ResVax预防60岁以上老年人RSV相关下呼吸道感染率为-7.9%。这也就意味着,ResVax不仅不能预防RSV,还会加重RSV。
Novavax并未就此放弃,但好运仍未降临。在另一项针对孕妇的临床试验中,ResVax预防下呼吸道感染率为39.4%,预防住院率为44%,均低于50%这一及格线。
这其实也不单单是ResVax一款疫苗的问题。
根据顶刊《新英格兰医学杂志》上的一篇研究,在对使用post-F作为抗原的RSV疫苗进行的五项三期试验中,没有一种疫苗能将中和活性提高5倍以上。最终,研究人员发现,post-F构象的蛋白抗原性较差,不足以激发足够强的保护效果。
好在,随着生物技术不断发展,研究人员开始掌握稳定pre-F蛋白的策略。上述三期临床成功的三款RSV疫苗,均选择了pre-F蛋白作为抗原。
辉瑞的RSV疫苗抗原,分别来自RSV A与RSV B病毒亚型的pre-F蛋白,是三款疫苗中唯一使用双价抗原的产品;葛兰素史克和Moderna的RSV疫苗抗原则均以DS-Cav1为基础。DS-Cav1是2013年中美科学家联合设计的pre-F抗原。
以DS-Cav1为基础的RSV疫苗设计,让人们看到了希望。不过,在重组蛋白的稳定性评价过程中,DS-Cav1的稳定性似乎并没有预期中乐观。于是,药企不得不寻求其他的pre-F结构设计来解决问题。
葛兰素史克的疫苗,是基于DS-Cav1的序列基础,通过引入半胱氨酸残基稳定在其融合前构象,形成二硫键,从而稳定蛋白质的构象或寡聚状态;Moderna则选择在DS-Cav1的基础上,增加两个位点突变,使得DS-Cav1三聚体的单体之间增加了额外的二硫键,让三聚体结构更稳定。
正是抗原从post-F蛋白到pre-F蛋白的改变,才将RSV疫苗从屡战屡败的深渊中拯救出来。
02 至关重要的佐剂
虽然辉瑞和葛兰素史克的RSV疫苗都选择pre-F蛋白作为抗原,但同为重组蛋白疫苗,二者的效果仍有不小的差距。这又是为什么?
问题或许出在了佐剂上。对于重组蛋白疫苗而言,影响疫苗效果的除了抗原还有佐剂。抗原决定了所诱导免疫应答的特异性和靶向性,佐剂则决定了免疫应答的强度。
在疫苗配方中加入佐剂可以增强疫苗的效果,并降低抗原浓度和保护效果所需的免疫次数。
拿葛兰素史克的RSV疫苗来说,在临床试验中,葛兰素史克分别评估不使用佐剂、使用AS01e、ASO1b佐剂对RSV疫苗的安全性和有效性的影响。
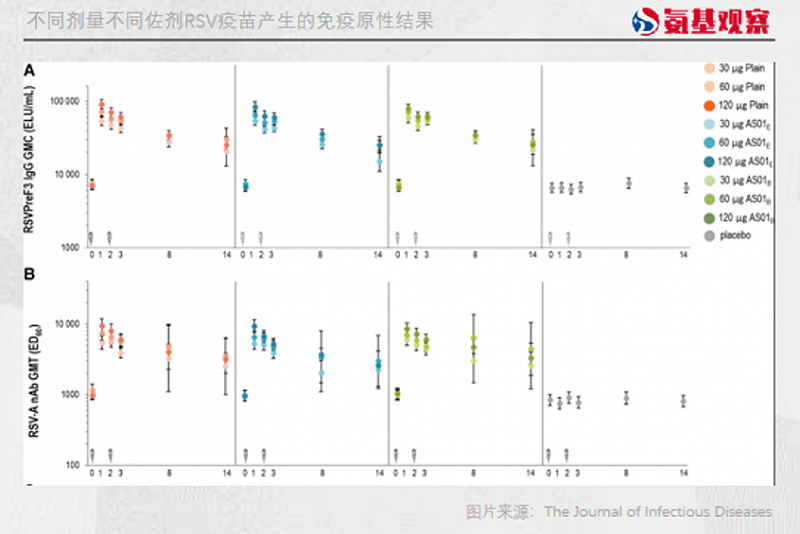
结果显示,与无佐剂相比,任何佐剂的存在显著增加了体液免疫和细胞免疫。其中,使用AS01b佐剂RSV疫苗的免疫原性,比使用AS01e的免疫原性更高。不过,鉴于AS01e出现的不良反应更低,最终葛兰素史克在RSV疫苗中选择了AS01e这一佐剂。
再看辉瑞的RSV疫苗,其也进行过两项临床试验。分别在RSV疫苗中加入铝佐剂Al(OH) 3、 CpG/Al(OH) 3佐剂。不过,结果显示,两种佐剂均未给RSV疫苗带来更强的效果。基于这一结果,辉瑞的RSV疫苗选择了不使用佐剂。
正如前文所说,佐剂之于重组蛋白疫苗很重要,那么,为什么在葛兰素史克和辉瑞的试验中,佐剂所发挥的作用却如此不同?造成这一差距的原因,或许在于它们选择的佐剂不同。
我们都知道,疫苗的抗原应答可以分为Th1和Th2两种,Th1型应答主要导致细胞介导的免疫反应,Th2型应答是能够诱导中和抗体反应的体液免疫。
而传统的铝佐剂通常只能诱导Th2型应答,但仅这一种类型的免疫应答,为疫苗提供的保护效率并不算高。
葛兰素史克的AS01佐剂则能诱导强大的特异性辅助CD4 + T细胞反应,还能与蛋白质结合时快速持久的体液和细胞反应,自然也就能带来更好的保护效果。这在其重组带状疱疹疫苗Shingrix中,已经得到验证。97.2%的超高保护率让Shingrix直接取代两默沙东的Zostavax。
那么,辉瑞为何不选择更好的佐剂?或许是因为,辉瑞意在将其RSV疫苗适用群体扩大到孕妇,所以其也只能选择安全性较好的铝佐剂进行试验。
RSV疫苗再一次让我们看到了,新型佐剂之于重组蛋白疫苗的重要性。
03 速度与效果的研发竞赛
RSV疫苗的研发能够走到今时今日,着实不易。
回顾RSV疫苗的研发经历,可以说是一部屡战屡败的血泪史。过去,人类在这一疫苗的研发上花去了60多年时间,辉瑞、Novavax、葛兰素史克都曾在这一领域摔倒。
尤其是Novavax,曾一度因RSV疫苗的接连失败,差点面临破产危机。好在,经过一家家药企前赴后继的研究,如今RSV疫苗距离上市仅有一步之遥。
而几乎在同一时间点撞线的三款RSV疫苗,必将有一场残酷的正面对决。谁能够有着更好的安全性、有效性,谁就拥有更大的想象空间。
海外三巨头肉搏,国内却是另一番景象。目前,国内RSV疫苗玩家寥寥无几,进度最快的是艾棣维欣的BARS13,处于二期临床阶段。
这也意味着,国内RSV疫苗仍然有着巨大的想象空间。毕竟,不同于海外玩家的摸黑走路,海外药企已经为国内药企指明了RSV疫苗的研发方向。
一款高效RSV疫苗所必须具备的特质,包括强大的佐剂、稳定的pre-F蛋白抗原。
都说失败乃成功之母,就像新冠疫苗研发如此之快,RSV疫苗也有一定功劳。同为冠状病毒,某种程度上,RSV疫苗失败的开发积累,也为新冠疫苗研发提供了大量的参考经验。
而对于国内疫苗企业来说,与其在热门疫苗领域挤破头颅也难分得一杯羹,在RSV这一高难度疫苗领域蓄力,也不失为另一种不错的选择。
当然,一旦入局,等待它们的将是又一场关于速度与效果的研发竞赛。